|
华盛顿 大学医学院 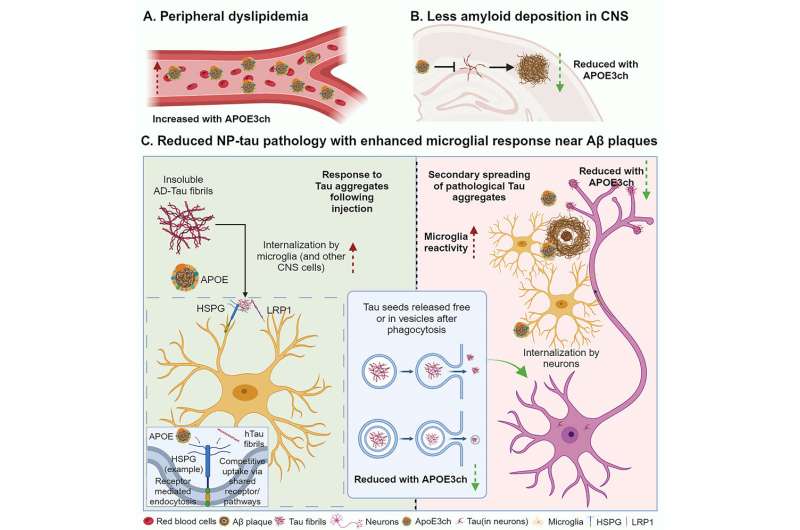 阿尔茨海默氏症已经困扰哥伦比亚一个大家庭几代人,导致半数年富力强的成员死亡。但这个家庭的一名成员逃脱了看似命运的命运:尽管她遗传了导致她的亲戚在 40 多岁时患上痴呆症的基因缺陷,但她的认知能力一直保持健康,直到 70 多岁。
圣路易斯华盛顿大学医学院的研究人员现在认为他们知道原因了。之前的一项研究报告称,与她的亲戚不同,这名妇女携带了两份 APOE 基因的罕见变体,即克赖斯特彻奇突变。
在这项研究中,研究人员使用转基因小鼠证明,克赖斯特彻奇突变切断了阿尔茨海默氏病早期(一种称为β淀粉样蛋白的蛋白质在大脑中积聚)和晚期(另一种称为 tau 的蛋白质积聚和认知能力开始下降。因此,尽管这位女士的大脑中充满了大量的淀粉样蛋白,但她几十年来仍保持思维敏锐。该研究结果于 12 月 11 日发表在《细胞》杂志上,提出了一种预防阿尔茨海默氏痴呆症的新方法。 “任何保护性因素都非常有趣,因为它为我们提供了了解这种疾病如何发生的新线索,”资深作者、芭芭拉·伯顿和鲁本·M·莫里斯三世神经病学杰出教授大卫·M·霍尔茨曼医学博士说。 “随着人们年龄的增长,许多人的大脑中开始积累一些淀粉样蛋白。最初,他们的认知能力保持正常。然而,多年后,淀粉样蛋白的沉积开始导致 tau 蛋白的积累。当这种情况发生时,认知障碍很快就会出现如果我们能找到一种方法来模仿 APOE 基因突变的影响,我们也许能够阻止那些已经患上阿尔茨海默氏痴呆症的人继续走这条路。”
阿尔茨海默病的发病过程大约需要 30 年。前二十年左右是沉寂的;淀粉样蛋白在大脑中缓慢积累,不会造成不良影响。然而,当淀粉样蛋白水平达到临界点时,它们就会启动第二阶段,其中涉及多个相互关联的破坏过程:一种名为 tau 的蛋白质形成缠结,并在大脑中扩散;大脑新陈代谢减慢,大脑开始萎缩;人们开始出现记忆和思维问题。这种疾病在遗传性和非遗传性阿尔茨海默病患者中遵循相同的模式。
这些哥伦比亚家庭携带一种名为早老素-1 (presenilin-1) 的基因突变,导致他们的大脑从 20 多岁开始就产生过多的淀粉样蛋白。携带这种突变的人淀粉样蛋白积累得如此之快,以至于他们达到了临界点,并在中年开始表现出认知能力下降的迹象。一个罕见的例外是,一名 70 多岁的女性大脑中的淀粉样蛋白含量比她 40 多岁时的亲戚还要多,但脑损伤和认知障碍的迹象非常轻微。 “阿尔茨海默氏症领域最大的悬而未决的问题之一是为什么淀粉样蛋白积累会导致tau 蛋白病理学,”Holtzman 说。“这位女士非常非常不寻常,因为她患有淀粉样蛋白病理,但没有太多 tau 蛋白病理,并且仅出现晚期出现的非常轻微的认知症状。这向我们表明,她可能掌握了淀粉样蛋白和 tau 蛋白之间联系的线索。” 2019 年的一项研究表明,除了 presenilin-1 突变外,该女性的 APOE 基因(另一种与阿尔茨海默病相关的基因)的两个拷贝也都携带基督城突变。但由于世界上只有一个人拥有这种特殊的基因突变组合,因此没有足够的数据证明基督城的突变是她对阿尔茨海默病具有显着抵抗力的原因,而不仅仅是一个巧合的发现。 为了解决这个难题,霍尔兹曼和第一作者陈云(研究生)转向转基因小鼠。他们选取了基因上容易过度产生淀粉样蛋白的小鼠,并对它们进行改造,使其携带带有克赖斯特彻奇突变的人类 APOE 基因。然后,他们将少量的人类 tau 蛋白注射到小鼠大脑中。通常,将 tau 蛋白引入已经充满淀粉样蛋白种子的大脑中会发生一种病理过程,其中 tau 蛋白在注射部位聚集成聚集体,然后这种聚集体扩散到大脑的其他部位。 对于带有基督城突变的小鼠来说,情况并非如此。与哥伦比亚妇女非常相似,尽管存在大量淀粉样斑块,这些小鼠仍出现了轻微的 tau 蛋白病变。研究人员发现,关键的区别在于小胶质细胞(大脑的废物处理细胞)的活动水平。小胶质细胞倾向于聚集在淀粉样斑块周围。在携带 APOE Christchurch 突变的小鼠中,淀粉样斑块周围的小胶质细胞加速并高效地消耗和处理 tau 蛋白聚集物。 Holtzman 说:“在 tau 蛋白病理学有效扩散到下一个细胞之前,这些小胶质细胞会吸收 tau 蛋白并将其降解。” “这阻碍了大部分下游过程;如果没有 tau 病理学,你就不会出现神经变性、萎缩和认知问题。如果我们能够模仿突变所产生的影响,我们也许能够使淀粉样蛋白的积累变得无害,或者至少危害要小得多,并且可以保护人们免受认知障碍的影响。” (责任编辑:泉水) |
基因突变可以预防阿尔茨海默病的发生
时间:2023-12-13 23:38来源:Medicalxpress 作者:泉水
顶一下
(0)
0%
踩一下
(0)
0%
------分隔线----------------------------
- 发表评论
-
- 最新评论 进入详细评论页>>
- 推荐内容
-
- 人工智能可提前两年预测老年痴呆
麦吉尔大学的人工智能研究成果,用不了多久就可以让世界各地...
- 中国科学家发现老年痴呆与人体铁
中国科学家的一项最新研究发现,老年痴呆症患者血清铁含量显...
- 英呼吁对痴呆症发起“全球反击”
八国集团卫生部长11日齐聚伦敦,共商痴呆症应对策略。英国首...
- 老年痴呆应该如何治疗
老年痴呆应该如何治疗?老年痴呆预防?老年痴呆西医治疗?老...
- 慢性老年痴呆症怎样治疗效果最好
请问发病原因,症状如何,怎样治疗? 治疗效果 老年痴呆症 发病原...
- 怎样预防老年痴呆症的发生(之五
老年性痴呆的预防要从中年开始做起,因为老年性痴呆能如在痴...
- 人工智能可提前两年预测老年痴呆
