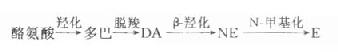|
第三节 肾上腺功能紊乱的临床生化 肾上腺是由中心部的髓质和周边部的皮质两个独立的内分泌器官组成。下面将分别讨论肾上腺髓质和皮质的内分泌功能紊乱的临床生化有关内容。 一、肾上腺髓质激素及功能紊乱 ㈠肾上腺髓质激素 肾上腺髓质从组织发育学上可看做是节后神经元特化为内分泌细胞(嗜铬细胞)的交感神经节,不同的嗜铬细胞可分别合成释放肾上腺素(epinephrine,E)、去甲肾上腺素(norepinephrine,NE)、多巴胺(dopamine,DA),三者在化学结构上均为儿茶酚胺类。后两者亦为神经递质,但作为递质释放的NE和DA绝大部分又重新被神经末梢及其中的囊泡主动摄取、贮存。肾上腺髓质释放的E约为NE的4倍,仅分泌微量DA,因此血液及尿液中的E几乎全部来自肾上腺髓质分泌,NE及DA则还可来自其他组织中的嗜铬细胞及未被摄取的神经递质。 儿茶酚胺类激素以酪氨为原料,经下列酶促反应生成。由于各种组织中存在的酶有不同,故分别合成E、NE或DA。
肾上腺髓质合成的E和NE贮存于嗜铬细胞的囊泡中,其释放受交感神经兴奋控制。作为激素释放的E和NE,亦具有交感神经兴奋样心血管作用及促进能量代谢、升高血糖等作用。进入血液的E和NE均迅速被单胺氧化酶及儿茶酚胺氧位甲基转移酶等代谢灭活,与临床生化检测有关的主要代谢产物如下:
㈡肾上腺髓质嗜铬细胞瘤及其临床生化诊断 肾上腺髓质嗜铬细胞瘤(pheochromocytoma)最好发部位。由于过量的E及NE释放入血液中,作用于肾上腺素受体,产生持续性或阵发性高血压,并伴有血糖、血脂肪酸、基础代谢率升高等代谢紊乱。本病的临床生化检查主要有两类。 ⒈儿茶酚胺类激素及其代谢物测定 由于检测技术限制,早年主要用比色法或荧光光度法测定24h尿中总游离儿茶酚胺类物质或VMA量。正常成人24h尿游离儿茶酚胺类物质总量<1.65μmol/d(280μg/d),VMA量为15.7-88.5μmol/d(3.1-17.6mg/d),二者明显超过正常值上限有助于嗜铬细胞瘤诊断。但血和尿中儿茶酚胺类主要为递质性NE及DA,而VMA为NE及E共有的代谢物,因此这两项指标对嗜铬细胞瘤,特别是发生于肾上腺髓质者特异性不高。并且该类测定影响因素多,香蕉、茶、咖啡等含香草的食品糖果、四环素、红霉素、多种拟肾上腺素药、抗抑郁症药及含多巴结构的药等可致假阳性;芬氟拉明、甲基葡胺造影剂可产生假阴性。随后采用检测仅为E代谢物的3-氧-甲基肾上腺素的24h尿排量,虽仍受上述因素影响,但特异性有所提高。3-氧-甲基肾上腺素的成人正常参考值范围为<5.07μmol/d。 近年来,由于采用HPLC-电化学检测法的灵敏度已可满足需要,故应用本法直接分离测定血浆中E及NE,对本病的诊断价值更高。但包括静脉穿刺取血在内的紧张及各种应急状态,甚至体位改变,均可刺激肾上腺髓质释放E及NE;而取血后室温下5min内不除去红细胞,将使E和NE浓度迅速下降。因此应在清晨平卧时,插入保留式静脉取血管(indwelling catheter),至少30min后待病人安静时再取血,转入盛有冰冻过的抗凝剂和抗氧化剂的试管中,迅速低温离心分离血浆进行测定。按上述条件测得的正常成人血浆参考值范围为E:109-437pmol/L(20-80pg/ml);NE:0.615-3.240nmol/L(104-548pg/ml)。嗜铬细胞瘤时,二者明显升高,若E升高较NE显著则提示可能为肾上腺髓质嗜铬细胞瘤。 ⒉动态功能试验诊断肾上腺髓质嗜铬细胞瘤的动态功能试验方法较多。目前兴奋试验常用胰高血糖素激发试验,即在疑为本病者非发作期,按上述步骤及方法取血及测量血压后,静脉注射胰高血糖素1mg,注毕每15s量血压,1-3min内再取血,分别测定给药前后血浆E及NE。由于胰高血糖素可迅速刺激肾上腺髓质释放E及NE,因此肾上腺髓质嗜铬细胞瘤者,血浆E和NE可较基础对照值升高明显,达3倍以上,血压也急剧上升,可达26.2/21.3kPa(200/160mmHg)。本法禁用于糖尿病人。抑制试验则多用可乐定(clonidine)抑制试验。降压药可乐定可抑制递质性儿茶酚胺释放,但不影响嗜铬细胞释放E及NE。对有高血压而怀疑本病者,给予可乐定0.3mg一剂口服前及服药后3h,分别取血测定血浆NE。非嗜铬细胞瘤性高血压者,血浆NE将降低50%以上,嗜铬细胞瘤性高血压者,NE仅轻度减少。本法尤适用于有持续性高血压,其他检测结果又在边缘范围者。由于多种降压药及三环类抗抑郁药可干扰本试验,故需停用上述药至少12h后才能进行。 二、肾上腺皮质的内分泌功能 ㈠肾上腺皮质激素及类固醇激素的生物合成 肾上腺皮质可分泌多种激素,按生理生化功能及分泌组织,可分做三类:①球状带分泌的盐皮质激素(mineralocorticoide),主要是醛固酮(aldosterone)和脱氧皮质酮(deoxycorticosterone);②束状带分泌的糖皮质激素(glucocorticoide),主要有皮质醇 (cortisol)及少量的皮质酮(corticosterone);③网状带分泌的性激素,如脱氢异雄酮(dehydroepiandrosterone)、雄烯二酮(androstenodione)及少量雌激素。从化学结构上看,这三类激素及性腺合成的其他性激素,均是胆固醇的衍生物,故统称类固醇激素(steroid hormones),而上述三类肾上腺皮质激素又合称皮质类固醇(corticosteroids)。 类固醇激素在人体内均是以胆固醇为原料,经过一系列酶促反应而合成的,只是由于某些酶活性在某些内分泌腺或同一腺体不同的组织中特别高,从而生成不同的激素。类固醇激素的主要合成途径及产物见图12-3。图中标示出了酶活性存在腺体差异性的反应步骤,以及临床常见的先天性酶缺陷所影响的步骤,有助于有关酶缺陷的临床生化诊断参考。 有关盐皮质激素的临床生化在第五章已作介绍,性激素的临床生化将在本章第五节讨论,故本节将只介绍有关糖皮质激素的临床生化。 ㈡糖皮质激素的运输及代谢 释放入血液中的糖皮质激素主要为皮质醇及10%左右的皮质酮。二者均约75%左右与肝脏合成的一种α1-球蛋白,即皮质素转运蛋白(transcortin),亦称皮质类固醇结合球蛋白(corticosteroid-binding globulin,CBG)可逆结合,15%与白蛋白可逆结合,仅10%左右以游离形式存在。CBG对糖皮质激素的亲和力高,但每分子CBG仅有一个结合部位,且血浆浓度低,故其结合容量有限。白蛋白虽然与糖皮质激素亲和力低,但可有多个结合位点,血浆浓度又高,因此结合容量大。当血中皮质激素浓度明显升高时,与CBG结合易达饱和,将出现与白蛋白结合部分及游离部分比率不成比例的升高。只有游离糖皮质激素才能进入靶细胞发挥生理生化作用及反馈调节自身分泌。 糖皮质激素的代谢主要在肝细胞中进行。主要反应方式为C-3酮基及环节中双键被加氢还原,生成多种加氢代谢物,以四氢皮质醇最多,此外尚有少量二氢、六氢代谢物。90%氢化皮质醇等代谢物及少量原型糖皮质激素,与葡糖醛酸或硫酸结合成相应的酯化物,从尿中排出,亦有少量可随胆汁排入肠道随着粪便排泄。以游离原型从尿中排出的皮质醇仅为血液总量的1%左右。
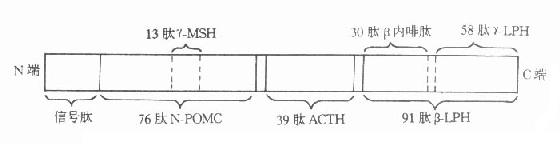
图12-3 类固醇激素生物合成的途径 ㈢糖皮质激素的生理生化功能 游离皮质醇等糖皮质激素可经靶细胞扩散入胞质内,与其受体结合。糖皮质激素-受体复合物转运入细胞核内,可启动某些DNA片段转录,生成的mRNA进入胞质,指导合成特异的酶和脂皮素(lipocortin)等蛋白质或肽类介质,产生广泛的生理生化作用。生理性浓度下,糖皮质激素的主要功能为: ⒈调节糖、脂肪、蛋白质三大营养物质的代谢 对糖代谢,糖皮质激素可促进糖原异生,增加肝糖原和肌糖原含量,另一方面又抑制除脑和心脏外其他组织对糖的利用,使血糖升高。对蛋白质代谢,可促进除肝脏外多种器官、组织的蛋白质分解,抑制蛋白质的合成,升高血中氨基酸,出现尿酸、尿素氮排泄增多等负氮平衡表现。糖皮质激素能激活四肢皮下的脂酶,促进这些部位的脂肪分解,血脂肪酸升高,并使脂肪呈向心性重新分布。 ⒉影响水电解质代谢 糖皮质激素有弱的盐皮质激素样潴钠排钾作用,亦有弱的促尿排钙排泄及抗利尿激素作用。 ⒊允许作用(permissible action) 机体内其他一些激素、神经递质等生物活性物质的作用,需有适当浓度的糖皮质激素存在,才能正常表达,此即糖皮质激素的“允许作用”。主要为对肾上腺素及胰高血糖素的作用。 但高浓度的糖皮质激素如药用或肾上腺皮质功能亢进等,则除上述作用增强外,还可表现出抑制炎症、免疫反应,影响血细胞等作用,将在肾上腺皮质功能亢进症中介绍。 ㈣糖皮质激素分泌的调节 和甲状腺激素分泌调节相似,肾上腺糖皮质激素的合成和分泌亦主要受图12-1所示的下丘脑-垂体-内分泌腺调节轴的控制。血液中游离糖皮质激素水平的变化,负反馈地引起下丘脑及垂体分别释放促肾上腺皮质激素释放激素(corticotropin releasing hormone,CRH)和促肾上腺皮质激素(corticotropin 或adrenocorticotropic hormone,ACTH)的增多或减少。CRH为下丘脑产生的一种含41个氨基酸残基的多肽,可选择性地促进腺垂体释放ACTH。ACTH是腺垂体促肾上腺皮质素细胞释放的39肽激素,可通过作用于肾上腺皮质束状带或网状带细胞膜上的ACTH受体,激活腺苷酸-cAMP-蛋白激酶系统,促进细胞增殖,合成和分泌糖皮质激素、性激素增多。持续的高ACTH状态仅早期一过性地引起盐皮质激素分泌增加,无持久影响。ACTH和CRH亦可负反馈地调节下丘脑CRH的释放。和甲状腺激素分泌调节不同,在肾上腺皮质激素的分泌调节中,最主要的是血液中游离糖皮质激素对下丘脑CRH释放的负反馈调节。ACTH和糖皮质激素的分泌存在明显的昼夜节律,分泌高峰见于晨6-8小时,低谷在午夜22-24时。此外,糖皮质激素是机体应激反应时释放的主要激素,因此,各种伤害性刺激均可通过高级神经中枢-下丘脑-垂体-肾上腺皮质轴,促进糖皮质激素的分泌。 除垂体外,一些垂体外的肿瘤主要是肺燕麦细胞癌,其次为胸腺癌、胰岛细胞癌、类癌、甲状腺髓样癌、嗜铬细胞瘤等,亦可分泌异源性ACTH。但这些异位肿瘤ACTH的分泌既不受血液糖皮质激素水平的负反馈调控,也不受CRH促进。此外,近年还发现有少数肿瘤可不受糖皮质激素反馈调节地释放异源性CRH。 现已明确,无论是腺垂体还是异位肿瘤分泌的ACTH,均和γ-黑色细胞刺激素(γ-melanocyte stimulating hormone,γ-MSH)、β-促脂解素(β-lipotropic hormone,β-LPH)、β-内啡肽(β-endophin)等,来自同一由265个氨基酸残基组成的大分子前体蛋白,称阿片皮质素原(proopiomelanocortin,POMC)。ACTH等有关多肽激素与POMC的关系见图12-4。
图12-4 阿片皮质素原及其多肽激素裂解产物的关系 三、肾上腺皮质功能紊乱 ㈠皮质醇增多症 皮质醇增多症(hypercortisolism)又称库欣综合征(Cushing’s syndrome),是各种原因致慢性糖皮质激素分泌过多而产生的症候群统称。按病因可分做:①垂体腺瘤及下丘脑-垂体功能紊乱,ACTH过量释放产生的继发性皮质醇增多症,又称库欣病,约占70%。其中主要为不伴蝶鞍扩大的微腺瘤,其病因定位诊断主要依赖临床生化检测。②肾上腺皮质肿瘤或结节性增生所致的原发性者,其中以皮质腺瘤多见,约占总病例的近20%,皮质腺瘤约占5%,结节性增生少见。此类病人糖皮质激素分泌一般呈自主性,不受ACTH调控。③异源性ACTH或CRH综合征,由垂体、下丘脑以外的癌瘤细胞分泌释放异源性ACTH或CRH而致。前者以肺燕麦细胞癌最多见,其次为胸腺癌、胰岛细胞癌等;后者可见于肺癌及类癌。早年统计,异源性ACTH、CRH综合征约占皮质醇增多症的5%,但随着对此症的警惕及诊断手段提高,近年发现发病率上升,甚至有报告高达占皮质醇增多症20%的。此外,药源性皮质醇增多症虽临床常见,但因有明确的大剂量糖皮质激素应用史可查,不在此讨论。 (责任编辑:泉水) |
第三节 肾上腺功能紊乱的临床生化
时间:2006-07-22 22:14来源:大众医药网 作者:admin
顶一下
(3)
100%
踩一下
(0)
0%
------分隔线----------------------------
- 发表评论
-
- 最新评论 进入详细评论页>>